|
 Virus:
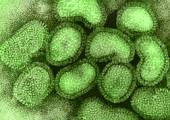
Virus:
En su fase intracelular el virus existe en forma de ácido nucleico (DNA o RNA) en replicación. Durante esta fase la célula huésped no sólo lleva a cabo la replicación del material genético del virus, sino que lo utiliza como mensaje genético para la síntesis de proteínas específicas del virus. Entre estas proteínas se encuentran las subunidades o capsómeros que, una vez ensamblados, constituyen la cápsida de la partícula vírica o virión.
A la partícula vírica o virión, se la llama también partícula infecciosa porque es la única que al salir del interior de una célula parasitada puede penetrar en una célula sana, lográndose así la transmisión de la infección de célula a célula. La mayor parte de los virus que se conocen son citolíticos, es decir producen la lisis y muerte de las células que infectan. Otras especies víricas no producen la muerte celular después de la infección sino que producen la transformación celular y estimulan de forma no controlada su división, originando un tumor.
El sistema de clasificación más extendido (Lwoft et al, 1962) agrupa a los virus según sus características químicas y estructurales, propiedades que se mantienen constantes y que se pueden determinar con precisión: tipo de ácido nucleico, arquitectura de la cápsida, presencia o ausencia de envoltura y tamańo de la cápsida. En este sistema de clasificación el papel del huésped juega un papel secundario.
Otro sistema de clasificación se basa en la capacidad de infectar determinadas células huésped y de acuerdo con ello se subdividen en tres clases principales: virus animales, virus bacterianos o bacteriófagos y virus de las plantas.
Retrovirus:
Virus con envoltura que presentan un genoma de ARN monocatenario y se replican de manera inusual a través de una forma intermedia de ADN bicatenario. Este proceso se lleva a cabo mediante la enzima retrotranscriptasa o transcriptasa inversa, que dirige la síntesis de ADN a través de ARN y posee una importancia extraordinaria en la manipulación genética. Una vez se ha pasado de ARN monocatenario a ADN se inserta dentro del ADN propio de la célula infectada donde se comporta como un gen más.
 Retrovirus humanos:
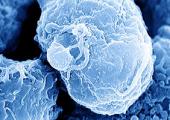
Retrovirus humanos:
Existen 4 retrovirus humanos identificados: el virus de la inmunodeficiencia humana de tipo 1 (VIH-1), el de tipo 2 (VIH-2) y los virus linfotrópicos de células T humanos de tipo I y II (HTLV-I y HTLV-II). Todos tienen como diana los linfocitos T. Los virus de la inmunodeficiencia humana producen la lisis de las células que infectan provocando una severa inmunodepresión. Los virus HTLVI/ II producen la inmortalización de los linfocitos infectados, generando una replicación descontrolada de los mismo, y por lo tanto una linfoproliferación. VIH-1: el síndrome de inmunodeficiencia humana o SIDA, es la expresión final de la infección por el VIH. La infección por este virus ocasiona la destrucción del sistema inmunitario además de manifestaciones neurológicas y tumorales. Estas manifestaciones clínicas se debe al tropismo tanto macrofágico como linfocitario del virus6. Presenta una preferencia para infectar a linfocitos TCD4+7, 8 en los que la replicación es activa y muy agresiva, lo que provoca como característica de la infección una profunda inmunosupresión. La fisiopatología del SIDA es un proceso complejo, donde existen implicados mecanismos patogénicos tan diferentes que algunos hasta hoy no han sido completamente comprendidos.
Citosol: Es el medio acuoso del citoplasma en el que se encuentran inmersos los orgánulos celulares. Representa aproximadamente la mitad del volumen celular. Contiene gran cantidad de proteínas, la mayoría enzimas que catalizan un gran número de reacciones del metabolismo celular. En él se llevan a cabo las reacciones de la glucólisis (degradación de la glucosa) y las de la biosíntesis de azúcares, de ácidos grasos, de aminoácidos y de nucleótidos. Contiene gran variedad de filamentos proteicos que le proporcionan una compleja estructura interna.
 Seguridad:
Seguridad:
El Real Decreto 664/1997, sobre los riesgos relacionados con la exposición agentes biológicos establece para el trabajo con microorganismos, así como para aquellas actividades que implican la manipulación de animales vertebrados infectados de forma natural o deliberadamente, cuatro niveles de contención o de bioseguridad. Estos niveles de seguridad son equivalentes a los recomendados por organismos como el Center for Disease Control (CDC), Atlanta, USA, y se tratan ampliamente en la NTP 468 (Trabajo con animales de experimentación). A cada agente vírico corresponde un nivel de contención previamente asignado.
Nivel de contención 4:
La unidad animal estará situada en un edificio separado o dentro de una zona claramente aislada en el interior del edificio. Si hay aberturas, deberán estar selladas. Será obligatorio un vestuario de doble zona con ducha en cada entrada.
Las conducciones eléctricas, luminarias, bocas y conductos de aspiración, deberán concebirse de manera que la deposición de polvo sea la mínima posible. Los circuitos de ventilación deben ser totalmente estancos y las puertas de la unidad deberán poder cerrarse con llave. Una seńal debe indicar cuando los animales infecta dos estén presentes en el interior de la misma.
El sistema de ventilación ha de ser autónomo, ha de mantener una depresión controlada, siempre circulando de la zona menos contaminada hacia las zonas de mayor contaminación. El aire extraído se filtrará a través de filtros HEPA y deberá expulsarse al exterior lejos de todas las bocas de aspiración de aire. Un sistema de alarma advertirá de cualquier fallo en el funcionamiento.
El aire expulsado de las cabinas de seguridad, si se filtra a través de filtros HEPA, se podrá expulsar al exterior por el conducto de evacuación general. Si no es así, debe hacerse pasar a través de los filtros principales de trata miento de aire antes de expulsarse al exterior. Deben tomarse precauciones durante el cambio de los filtros, llevando a cabo su descontaminación previa y emplean do ropa de protección.
 Cabinas de Seguridad Biológica. Clase III:
Cabinas de Seguridad Biológica. Clase III:
Está herméticamente sellada, separando completamente al trabajador del trabajo que esté realizando mediante barreras físicas (panel frontal completamente cerrado, manipulación a través de guantes de goma). El aire es tomado del local o del exterior y filtrado. En su extracción (100%), suele haber dos filtros HEPA montados en serie para la completa purificación del aire extraído. Preferiblemente la descarga de aire se efectuará al exterior, de este modo, a pesar de que el aire extraído es microbiológicamente limpio, se consigue una seguridad adicional que consiste en el factor de dilución atmosférico en los casos en que se produzcan fallos en el sellado de los filtros o en los propios filtros.
En los casos en que la descarga se haga en el interior de los locales hay que tener en cuenta que en función de los materiales manipulados, partículas de diámetro inferior a 0,3 µ, pueden no ser retenidas por los filtros HEPA, por lo que deberá incorporarse un sistema complementario de tratamiento del aire extraído.
Se utilizan para el trabajo con agentes biológicos de los grupos 3 y 4, que causan enfermedades humanas graves. Puede existir el riesgo de que se propague en la colectividad y (grupo 4) no se suele disponer de profilaxis o tratamientos efectivos. También sirven para compuestos químicos tóxicos y/o cancerígenos, siempre y cuando se modifique el sistema de tratamiento del aire expulsado según las normas.
Es aconsejable realizar una limpieza y desinfección de las superficies de las Cabinas antes de iniciar el trabajo. El uso de aspiradores eliminará el polvo acumulado durante el montaje y transporte. La desinfección se realiza con una solución bactericida de elevado poder esterilizante, o bien empleando alcohol al 70% (alcohol isopropílico).
La limpieza y desinfección de la Cabina se efectua antes de cualquier trabajo de mantenimiento rutinario o accidental de la Cabina, antes de realizar un test de control mecánico o biológico en la zona de trabajo, antes de empezar a trabajar, siempre que se cambie de programa de trabajo y en caso de que se haya producido un derramamiento de líquido en la mesa de trabajo. Las partes de la Cabina que están contaminadas (ventiladores, plenos, filtros, etc.) y que no son accesibles en operaciones normales de limpieza y desinfección, deben ser descontaminadas mediante esterilización gaseosa. El procedimiento más sencillo consiste en la depolimerización de paraformaldehido por calentamiento. Esta operación debe realizarse antes de trabajos de mantenimiento, antes del cambio de los filtros, antes de realizar los test básicos de control. Esaconsejable realizar la descontaminación antes del traslado de la Cabina, antes de cambiar el programa de trabajo y después de un derrame que contenga una alta concentración del agente manipulado
La descontaminación por el calor o con una solución descontaminante de eficacia comprobada es obligatoria para todos los efluentes líquidos: lavabo, aseo, ducha, sifón del WC y condensaciones del autoclave, que debe ser de doble puerta.
El acceso a los locales estará restringido únicamente al personal autorizado por el director, oída la opinión del servicio médico, informando de los riesgos, así como la manera como debe protegerse. El personal entrará y saldrá por el compartimento estanco del vestuario. La ropa de calle se quitará en la zona limpia y se colocará ropa de trabajo completa (guarda polvo, pantalón, camisa, calzado y guantes) al entrar al animalario. A la salida, esta ropa se quitará y se dejará en la zona de espera del animalario. Será obligatorio ducharse antes de ponerse la ropa de calle de nuevo. Es obligatoria una vigilancia médica especial para las personas que trabajan o que tienen acceso a la unidad animal, creándose una seroteca de dicho personal.
Deberán dictarse normas muy detalladas de la conducta que se debe seguir ante situaciones de emergencia (evasión de un animal, conato de incendio, fugas, vertidos, etc.). El personal de la unidad animal deberá ser informado sobre el cumplimiento de estas normas.
 Animales infectados:
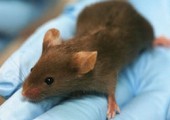
Animales infectados:
La investigación puede requerir disponer de animales deliberadamente infectados, con el correspondiente riesgo de contaminación. Debe tenerse en cuenta que los animales de experimentación pueden ser reservorios naturales de enfermedades de tipo infeccioso, producir alergias, ser fuente de accidentes a través de arańazos, mordeduras, picaduras, etc. Su manipulación presenta siempre un riesgo de exposición a agentes biológicos.
Reconstrucción del virus de la gripe de 1918:
Causada por un brote de Influenza virus A del subtipo H1N1 que mató entre 50 y 100 millones de personas entre 1918 y 1919.
En 2001 se reconstruyó por primera vez un virus de gripe con la secuencia del segmento NS del virus de 1918 y con la secuencia de un virus adaptado en ratones. Los investigadores reconstruyeron ese virus quimera y evaluaron su virulencia.
En 2005 se publicó en Science la historia la reconstrucción completa in vitro de este virus totalmente extinto.
La genética reversa se basa en la posibilidad de "rescatar" un virus de novo a partir de la expresión de su material genético. La expresión coordinada del genoma de un virus en una célula usando vectores de expresión permite que se produzcan todos los factores necesarios para la creación del virus.
La síntesis de la proteína hemaglutinina responsable de la epidemia de 1918 se obtuvo juntando ADN procedente del pulmón de una mujer inuit encontrada en la tundra de Alaska y de muestras preservadas de soldados estadounidenses de la I Guerra Mundial.
Su vuelta a la vida tuvo lugar en un laboratorio de bioseguridad de nivel 3, del CDC en Atlanta.
Los efectos del virus reconstruido fueron comprobados con ratones, embriones de pollo y células pulmonares humanas. Los embriones de pollo fueron afectados de forma similar al contacto con el virus aviario H5N1.
Ébola 2014-2015:
La peor epidemia apareció en diciembre de 2013. Provocó 28.637 contagios y 11.315 muertos.
Fue declarada emergencia de salud pública internacional en agosto de 2014.
Su fin fue oficialmente declarado en enero 2016, 42 días después de que el último paciente fuera dado de alta en Monrovia. Se inició con un brote que se extendió por Guinea, Liberia y Sierra Leona, llegó hasta Malí, Nigeria y Senegal e incluso saltó fuera del continente con casos puntuales en EE.UU. y Espańa.
Un misionero enfermo repatriado y la gestión del traslado y tratamiento fue objeto de duras críticas.
El mayor pico se vivió en el verano de 2014 y durante 2015 se fue extinguiendo lentamente.
Fue muy mal gestionada durante los primeros meses durante los cuales la ayuda humanitaria fue puesta en marcha muy lentamente.
El virus mostró una gran capacidad, desconocida hasta entonces, para resistir en el organismo de los supervivientes.
Espańa quedó en el puesto 23 de la lista de donantes.
Como los brotes se ocasionaban raramente y sólo en países pobres, el sector privado tenía poco incentivo comercial en invertir en investigación.
(*) Tras la invasión de Ucrania las principales empresas tecnológicas establecidas en Rusia, como Microsoft, IBM, Intel, Google y Apple, suspendieron sus operaciones en el país y vendieron sus filiales. Este vacío fue llenado principalmente por dos empresas rusas: Kaspersky Lab, cuyo fundador Eugene Kaspersky ascendió entre los millonarios del puesto 101 al 66 (+70% de riqueza estimada) gracias a los contratos gubernamentales, y Astra Group, cuyo fundador Denis Frolov entró en la lista de multimillonarios rusos en el puesto 121 al hacerse cargo del desarrollo de infraestructura de software para importantes corporaciones y entidades estatales rusas.
En febrero de 2025 muere en EE.UU. una nińa no vacunada de sarampión, la primera en una década.
Su madre participó en una entrevista con la organización antivacunas Children's Health Defense dirigida hasta hace poco por Robert F. Kennedy Jr.
Sobre sus otros cuatro hijos dijo: Tuvieron una recuperación realmente buena y rápida, atribuyendo su recuperación a los tratamientos no probados.
Varias de las afirmaciones que hizo sobre vacunas, riesgos, causas, respuestas inmunitarias y bondad de tratamientos alternativos son falsas.
La tasa de mortalidad por sarampión es de 1 a 3 por cada 1.000 nińos.
Una infección de sarampión tiene la capacidad de anular las respuestas inmunitarias desarrolladas contra otras infecciones [amnesia inmunitaria] ya que destruye las células T y B de memoria. Esto deja a las personas que se recuperan del virus más vulnerables a todos los demás gérmenes.
CHD y Kennedy han difundido sin cesar información errónea y peligrosa sobre la vacuna triple vírica, incluyendo que causa autismo (no lo causa) e incluso muertes (no lo causa).
Tras décadas de investigación y análisis, los científicos no han encontrado ninguna relación entre el autismo y las vacunas triple vírica ni con ninguna otra vacuna.
Antes del desarrollo de las vacunas contra el sarampión, el virus infectaba de 3 a 4 millones de personas al ańo, causando 48.000 hospitalizaciones. Unas 1.000 desarrollaron inflamación cerebral y entre 400 y 500 fallecieron.
Dos dosis de la vacuna MMR tienen una eficacia del 97% contra el sarampión y se considera que la protección dura toda la vida.
|